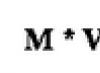Парциальным давлением ( p o ) газа в смеси называется давление, которое производил бы этот газ, занимая при тех же физических условиях объем всей газовой смеси.
Согласно закону: общее давление смеси газов, не вступающих друг с другом в химическое взаимодействие, равно сумме парциальных давлений газов, составляющих смесь.
Задачи
1. (Р.77) При н.у. масса 0,5×10 -3 м 3 газа равна 1,806*10× -3 кг. Определите плотность газа по диоксиду углерода СО 2 и метану СН 4 , а также молекулярную массу газа.
Ответ : 1,84, 5,05, 80,9 × 10 -9 кг.
2. (Р.83) Объем резиновой камеры автомобильной шины равен 0,025 м 3 , давление в ней 5,0665 × 10 5 Па. Определите массу воздуха, находящегося в камере, при 20°С.
Ответ : 0,15 кг.
3. (Р.86) Определите массу паров толуола в помещении объемом 30 м 3 при 25°С. Давление паров толуола при этой температуре равно 2972 Па.
Ответ : 3,31 кг.
4. (Р.88) Определите массу 10 -3 м 3 газовой смеси, содержащей (по объему) 50 % водорода и 50 % диоксида углерода (н.у.).
Ответ : 1,02 × 10 -3 кг.
5. (Р.89) Газ (н.у.) занимает объем 1 м 3 . При какой температуре объем газа утроится, если давление газа не меняется?
Ответ : 819 К.
6. (Р.92) Какую массу СаСО 3 надо взять, чтобы получить при его прокаливании диоксид углерода, занимающий объем 25 × 10 -6 м 3 при 15°С и давлении 104000 Па?
Ответ : 0,109 × 10 -3 кг.
7. (Р.94) Из 5 × 10 -3 кг хлората калия КСlО 3 было получено 0,7 × 10 -3 м 3 кислорода, измеренного при 20°С и давлении 111900 Па. Определите массовую долю примесей в хлорате калия.
Ответ : 48 %.
8. (С.1) Будет ли одинаковым количество молекул в равных объемах водорода и кислорода: а) при нормальных условиях; б) при температуре 25°С и давлении 1 атм; в) если условия, при которых измерены объемы водорода и кислорода, различны?
9. (С.9) При какой температуре 1 л хлора будет весить 1 г, если давление равно 1 атм?
Ответ : 863 К.
10. (С.15) Сосуд емкостью 112 л, заполненный воздухом под давлением 1 атм, весит 2,5 кг. Каков будет вес этого сосуда, если его наполнить хлором под давлением 5 атм?
Отве т: 4,13 кг.
11. (С.32) Литр одного газа, взятого при нормальных условиях, весит 1,43 г, второго – 0,09 г. Найдите число молекул во взятых объемах газа. Исключите лишние данные из задачи. Проведите расчет.
Ответ : 2,69 × 10 22 .
12. (С.35) Сколько молекул азота и кислорода будет находиться при нормальных условиях в 896 мл газовой смеси, состоящей по объему 50 % азота и 50 % кислорода? Исключите лишние данные из задачи. Проведите расчет.
Ответ : 2,41 × 10 22 .
13. (С.60) Определите плотность смеси окиси и двуокиси углерода по водороду, если известно, что окись углерода составляет 20 % по объему. Найдите массу 1 л такой смеси при температуре 27°С и давлении 1 атм.
Ответ : 20,4, 1,66 г.
14. (С.68) Объем смеси окиси углерода с кислородом равен 200 мл. После сгорания всей окиси углерода за счет находившегося в смеси кислорода и приведения объемов газов к первоначальным условиям было получено 150 мл новой смеси газов. Определите в процентах объемный состав исходной смеси.
Ответ : 50 %.
15. (С.76) Смесь водорода с азотом, объем которой измерен при определенных условиях, сожгли в избытке кислорода. После окончания реакции и приведения газов к первоначальным условиям (вода сконденсировалась) уменьшение объема газов оказалось равным объему исходной смеси водорода с азотом. Определите объемной соотношение газов в смеси.
Ответ : 2: 1.
16. (С.92) В замкнутом сосуде имеется 100 молей азота и водорода в отношении 1:3. Давление смеси 300 атм. Определите состав и давление смеси после того, как 10 % азота вступили в реакцию и газы приведены к первоначальной температуре.
Ответ : 285 атм.
17. (С.100) В замкнутом сосуде при температуре 0°С находилось 3 л кислорода и 4 л водорода. Как изменится давление в сосуде, если одно из веществ прореагирует полностью, после чего будет восстановлена первоначальная температура?
Ответ : в 7 раз.
18. (П.122) Какой из благородных газов находится в смеси с аммиаком, если известно, что при нормальном давлении и 80°С ее плотность равна 0,5165 г/л?
Ответ : Не.
19. (П.130) В смеси аммиака и азота число атомов в 3,4 раза больше числа молекул. Выясните относительную плотность этой газовой смеси по воздуху.
Ответ : 0,700.
20. (Г.21) Даны 480 л газа при 17°С и 104 кПа. Приведите объем газа к нормальным условиям: 0°С и 101,3 кПа.
Ответ : 464 л.
21. (Г.25) Даны 8 л газа при –23°С. При какой температуре объем газа станет равным 10 л, если давление останется неизменным?
Ответ : 39,5°С.
22. (Г.27) В закрытом баллоне находится газ при температуре –3°С под некоторым давлением. До какой температуры должен быть нагрет газ, чтобы давление внутри баллона выросло на 20 %?
Ответ : 51°С.
23. (Г.41) Баллон вместимостью 10 л содержит при 27°С моль кислорода. Вычислите давление кислорода в баллоне.
Ответ : 249 кПа.
24. (Г.42) В закрытом баллоне вместимостью 40 л находится 77 г СО 2 . Манометр, присоединенный к баллону, показывает давление 106,6 кПа. Вычислите температуру газа.
Ответ : 20,2°С.
25. (Г.56) Из 3 г смеси СаСО 3 и MgCО 3 получено 760 мл СО 2 (при 20°С и 99,7 кПа). Вычислите количественное соотношение СаСО 3 и MgCО 3 .
Ответ : 4:1.
26. (Г.58) Соединение содержит 46,15 % углерода, остальное – азот. Плотность по воздуху равна 1,79. Найдите истинную формулу соединения.
Ответ : C 2 N 2 .
27. (Г.67) При сжигании некоторого соединения азота с водородом полечено из 0,24 г Н 2 О и 168 мл азота (при 0°С и 101,3 кПа). Плотность пара азотсодержащего вещества по воздуху 1,1. Какова истинная формула вещества?
Ответ : N 2 H 4 .
28. (Г.128) Сколько молекул содержится в 1 мл любого газа, измеренного при нормальных условиях (при 0°С и 101,3 кПа)?
Ответ : 2,7 × 10 19 .
29. (Г.136) Сколько лет потребуется для того, счтобы пересчитать число молекул, которое содержится в 1 г воды, если отсчитывать по одной молекуле в секунду? (Считать год равным 365 дням).
Ответ : 1,06 × 10 15 .
30. (Р.96) При 0°С в сосуде объемом 14 × 10 –3 м 3 содержится 0,8 × 10 –3 кг водорода и 6,30 × 10 –3 кг азота. Определите парциальное давление азота и общее давление смеси.
Ответ : 36479,43; 101331,75 Па.
31. (Р.97) В газометре над водой при 20°С и давлении 98500 Па находится 8 × 10 –3 м 3 кислорода. Давление водяного пара при 20°С равно 2335 Па. Какой объем (н.у.) займет кислород, находящийся в газометре?
Ответ : 7,07 × 10 –3 м 3 .
32. (Р.98) Газовая смесь состоит из 5 × 10 –3 м 3 азота, находящегося под давлением 95940 Па, и 3 × 10 –3 м 3 кислорода. Объем смеси 8 × 10 –3 м 3 . Общее давление газовой смеси 104200 Па. Под каким давлением взят кислород?
Ответ : 117967 Па.
33. (Р.99) 0,2 × 10 –3 м 3 водорода собраны над водой при 33°С и давлении 96000 Па. Определите объем сухого водорода (н.у.). упругость насыщенного водяного пара при 33°С равна 5210 Па.
Ответ : 1,59 × 10 –4 м 3 .
34. (Р.100) В газонаполненных лампах содержится смесь газов, имеющая объемный состав: 86 % Ar и 14 % N 2 . Рассчитайте парциальное давление каждого из газов, если общее давление равно 39990 Па.
Ответ : 34391,4; 5598,6 Па.
35. (Р.101) Водород объемом 3 × 10 –3 м 3 находится под давлением 100500 Па. Какой объем аргона под таким же давлением надо прибавить к водороду, чтобы при неизменном общем давлении парциальное давление аргона в смеси стало равным 83950 Па?
Ответ : 15,2 × 10 –3 м 3 .
36. (Р.102) Газовая смесь составлена из 5 × 10 –3 м 3 метана под давлением 96000Па, 2 × 10 –3 м 3 водорода под давлением 84000Па и 3 × 10 –3 м 3 диоксида углерода под давлением 109000Па. Объем смеси 8 × 10 –3 м 3 . Определите парциальные давления газов в смеси и общее давление смеси.
Ответ : 60000; 21000; 40875; 121875 Па.
37. (Р.104) Равновесная смесь CO + Cl 2 « COCl 2 , содержащая 0,7 кмоль СО, 0,2 кмоль Cl 2 и 0,5 кмоль COCl 2 , находится под давлением 10 5 Па. Найдите парциальные давления газов в смеси.
Ответ : 50000; 14300; 35700 Па.
38. (Р.105) В закрытом сосуде объемом 6 × 10 –3 м 3 находится при 10°С смесь, состоящая из 8,8 × 10 –3 кг диоксида углерода, 3,2 × 10 –3 кг кислорода и 1,2 × 10 –3 кг метана. Вычислите общее давление газовой смеси, парциальные давления газов и их объемные доли (%).
Ответ : 147061,00; 78432,51; 39216,25; 29412,19 Па; 53,33; 26,67; 20 %.
39. (Г.69) Смешаны 4 г СН 4 и 24 г О 2 . Выразите состав газовой смеси в процентах по объему.
Ответ : 25 и 75 %.
40. (Г.70) Смешаны при нормальных условиях 56 л СН 4 и 112 л О 2 . Выразите состав газовой смеси в процентах по массе.
Ответ : 20 и 80 %.
41. (Г.71) Вычислите парциальные давления кислорода азота и кислорода в воздухе, приняв давление воздуха 101,3 кПа (воздух содержит 21 % О 2 и 78 % N 2 по объему).
Ответ : 21,3; 79 кПа.
42. (Г.72) Вычислите процентное содержание кислорода и азота в воздухе по массе. Масса 1 л воздуха (0°С и 101,3 кПа) составляет 1,293 г.
Ответ : 23,2 и 75,5 %.
43. (Г.75) Вычислите массу 70 мл кислорода, собранного над водой при 7°С и 102,3 кПа. Давление пара воды при той же температуре равно 1 кПа.
Ответ : 97,5 мг.
44. (Г.76) Какой объем займут 0,12 г кислорода, если собрать газ над водой при 14°С и 102,4 кПа. Давление пара воды при той же температуре составляет 1,6 кПа.
Ответ : 88,7 мл.
45. (Г.81) Сколько молей кислорода и азота содержится в аудитории размером 6´8´5 м при 22°С и 100,0 кПа?
Ответ : 2055 и 7635 моль.
46. (Г.83) В камеру вместимостью 1 м 3 заключили 15 моль N 2 , 25 моль СО 2 и 10 моль О 2 . Вычислите: а) общее давление смеси газов при 27°С; б) процентный состав смеси по массе; в) процентный состав смеси по объему; г) парциальное давление каждого из газов при заданной температуре.
Ответ : 125 кПа; 22,8; 59,8; 17,4 %; 30; 50 и 20 %; 37,4; 62,3; 24,9 кПа.
47. (Г.85) В каком объеме воздуха (0°С и 101,3 кПа) содержится 1 мг аргона? Воздух содержит 0,93 % аргона по объему.
Даже людям далеким от альпинизма и дайвинга известно, что дышать в определенных условиях человеку становится сложно. Такое явления связано со сменой парциального давления кислорода в окружающей среде, как следствие, и в крови самого человека.
Горная болезнь
Когда житель равнинной местности приезжает в отпуск в горы, кажется, что воздух там особенно чист и надышаться им просто невозможно.
На самом деле подобные рефлекторные позывы к частому и глубокому дыханию вызываются гипоксией. Чтобы человек выровнял парциальное давление кислорода в альвеолярном воздухе, ему требуется вентилировать собственные легкие как можно лучше первое время. Конечно, пребывая в условиях гор несколько дней или недель организм начинает привыкать к новым условиям за счет корректировки работы внутренних органов. Так ситуацию спасают почки, которые начинают выделять гидрокарбонат для усиления вентиляции легких и увеличивают в крови количество эритроцитов, способных переносить большее количество кислорода.
Таким образом, у жителей горных местностей уровень гемоглобина всегда оказывается выше, чем у равнинных.
Острая форма
В зависимости от особенностей организма норма парциального давления кислорода может отличаться для каждого человека в определенном возрасте, состоянии здоровья или просто от способности к акклиматизации. Именно поэтому покорять вершины суждено не всем, ведь даже имея огромное желание, человек не способен полностью подчинить себе свой организм и заставить его работать по-другому.
Очень часто у неподготовленных альпинистов при скоростном подъеме могут развиваться различные симптомы гипоксии. На высоте менее 4,5 км они проявляются головными болями, тошнотой, усталостью и резкой сменой настроения, поскольку нехватка кислорода в крови сильно отражается на работе нервной системы. Если подобные симптомы проигнорировать, то в дальнейшем образуется отек мозга или легких, каждый из которых способен привести к смерти.

Таким образом, игнорировать изменение парциального давления кислорода в окружающей среде строго запрещено, ведь оно всегда влияет на работоспособность всего человеческого организма.
Погружение под воду
Когда водолаз погружается в условия, где атмосферное давление ниже привычного уровня, его организм также сталкивается со своеобразной акклиматизацией. Парциальное давление кислорода на уровне моря является средней величиной и с погружением также меняется, но особую опасность для человека в данном случае представляет азот. На поверхности земли в равнинной местности он не влияет на людей, но после каждых 10 метров погружения постепенно сжимается и провоцирует в организме водолаза различные степени наркоза. Первые признаки такого нарушения могут проявляться уже после 37 метров под водой, особенно если человек проводит на глубине длительное время.

Когда атмосферное давление превышает 8 атмосфер, а достигается этот показатель уже после 70 метров под водой, водолазы начинают чувствовать азотный наркоз. Явление это проявляется ощущением алкогольного опьянения, которое нарушает координацию и внимательность подводника.
Чтобы избежать последствий
В случае, когда парциальное давление кислорода и других газов в крови отклонено от нормы и водолаз начинает ощущать признаки интоксикации, очень важно осуществлять его подъем максимально медленно. Связано это с тем, что при резком изменении давления диффузия азота провоцирует возникновение в крови пузырьков с данным веществом. Простым языком, кровь как будто закипает, и человек начинает чувствовать сильную боль в суставах. В дальнейшем у него могут развиваться нарушения зрения, слуха и работы нервной системы, что называют кессонной болезнью. Чтобы избежать такого явления, водолаза следует поднимать очень медленно или заменять в его дыхательной смеси азот гелием. Данный газ менее растворим, имеет меньшую массу и плотность, поэтому затраты на уменьшаются.
Если же подобная ситуация произошла, то человека необходимо срочно помещать в обратно среду с высоким давлением и ждать постепенной декомпрессии, которая может продолжаться до нескольких дней.
Для того чтобы изменился газовый состав крови, не обязательного покорять вершины или спускаться на морское дно. Различные патологии сердечно-сосудистой, мочевыделительной и дыхательной систем также способны влиять на изменение давления газов в главной жидкости человеческого организма.
Для точного определения диагноза у пациентов берутся соответствующие анализы. Чаще всего врачей интересует парциальное давление кислорода и углекислого газа, поскольку они обеспечивают полноценное дыхание всех органов человека.

Давление в данном случае представляет собой процесс растворения газов, который показывает, насколько эффективно в организме работает кислород и соответствуют ли его показатели нормам.
Малейшие отклонения указывают на то, что у пациента имеются отклонения, влияющие на способность использовать поступающие в организм газы по максимуму.
Нормы давления
Норма парциального давления кислорода в крови понятие относительное, поскольку может варьироваться в зависимости от множества факторов. Чтобы правильно определить свой диагноз и получить лечение, с результатами анализов необходимо обращаться к специалисту, способному учесть все индивидуальные характеристики пациента. Конечно, существуют и эталонные нормы, которые принято считать идеальными для здорового взрослого человека. Так, в крови пациента без отклонений имеется:
- углекислый газ в количестве 44,5-52,5 %;
- его давление 35-45 мм рт. ст.;
- насыщение жидкости кислородом 95-100 %;
- О 2 в количестве 10,5-14,5 %;
- парциальное давление кислорода в крови 80-110 мм рт. ст.
Чтобы во время сдачи анализа результаты соответствовали действительности, необходимо учесть целый ряд факторов, способных повлиять на их корректность.
Причины отклонения от нормы, зависящие от пациента
Парциальное давление кислорода в артериальной крови может меняться очень быстро в зависимости от различных обстоятельств, поэтому, чтобы результат анализа был максимально точным, следует учитывать следующие особенности:
- норма давления всегда уменьшается с увеличением возраста пациента;
- при переохлаждении снижается давление кислорода и давление углекислого газа, а уровень рН увеличивается;
- при перегреве ситуация обратная;
- действительный показатель парциального давления газов будет виден только при заборе крови у пациента с температурой тела в пределах нормы (36,6-37 градусов).

Причины отклонения от нормы, зависящие от медработников
Кроме учета таких особенностей организма самого пациента, специалисты для корректности результатов также должны соблюдать определенные нормы. В первую очередь на парциальное давление кислорода влияет наличие пузырьков воздуха в шприце. Вообще, любой контакт анализа с окружающим воздухом способен изменить результаты. Также важно после забора крови аккуратно перемешать ее в емкости, чтобы эритроциты не оседали на дне пробирки, что также способно сказаться на результатах анализа, демонстрирующих уровень гемоглобина.

Очень важно придерживаться и норм времени, отведенных на проведение анализа. По правилам, все действия должны осуществляться в пределах четверти часа после забора, и если этого времени недостаточно, то емкость с кровью должна помещаться в ледяную воду. Только так можно остановить процесс потребления кислорода клетками крови.
Специалисты также должны своевременно калибровать анализатор и брать анализы только шприцами с сухим гепарином, который сбалансирован электролитически и не оказывает влияния на кислотность пробы.
Результаты анализов
Как уже понятно, парциальное давление кислорода в воздухе способно оказывать на организм человека заметное влияние, но уровень давления газов в крови может нарушаться и по другим причинам. Чтобы определить их правильно, расшифровку следует доверять только опытному специалисту, способному учесть все особенности каждого пациента.
На гипоксию в любом случае будет указывать снижение уровня давления кислорода. Изменение уровня рН крови, как и давления углекислого газа или изменение уровня бикарбонатов, может указывать на ацидоз или алкалоз.
Ацидоз представляет собой процесс закисления крови и характеризуется повышением давления углекислого газа, снижением уровня рН крови и бикарбонатов. В последнем случае диагноз будет озвучен как метаболический ацидоз.

Алкалоз представляет собой повышение щелочности крови. О нем будет свидетельствовать повышенное давление углекислого газа, увеличение числа бикарбонатов, а следовательно, и изменение уровня рН крови.
Заключение
На работоспособность организма влияет не только качественное питание и физические нагрузки. Каждый человек привыкает к определенным климатическим условиям жизни, в которых чувствует себя максимально комфортно. Их изменение провоцирует не только плохое самочувствие, но и полную смену определенных показателей крови. Чтобы определить по ним диагноз, следует тщательно подбирать специалиста и следить за соблюдением всех норм забора анализов.
В обычных условиях человек дышит обычным воздухом, имеющим относительно постоянный состав (табл. 1). В выдыхаемом воздухе всегда меньше кислорода и больше углекислого газа. Меньше всего кислорода и больше всего углекислого газа в альвеолярном воздухе. Различие в составе альвеолярного и выдыхаемого воздуха объясняется тем, что последний является смесью воздуха мертвого пространства и альвеолярного воздуха.
Альвеолярный воздух является внутренней газовой средой организма. От его состава зависит газовый состав артериальной крови. Регуляторные механизмы поддерживают постоянство состава альвеолярного воздуха. Состав альвеолярного воздуха при спокойном дыхании мало зависит от фаз вдоха и выдоха. Например, содержание углекислого газа в конце вдоха всего на 0,2-0,3% меньше, чем в конце выдоха, так как при каждом вдохе обновляется лишь 1/7 часть альвеолярного воздуха. Кроме того, протекает непрерывно, при вдохе и при выдохе, что способствует выравниванию состава альвеолярного воздуха. При глубоком дыхании зависимость состава альвеолярного воздуха от вдоха и выдоха увеличивается.
Таблица 1. Состав воздуха (в %)
Газообмен в легких осуществляется в результате диффузии кислорода из альвеолярного воздуха в кровь (около 500 л в сутки) и углекислого газа из крови в альвеолярный воздух (около 430 л в сутки). Диффузия происходит вследствие разности парциального давления этих газов в альвеолярном воздухе и их напряжений в крови.
Парциальное давление газа: понятие и формула
Парциальное давленые газа в газовой смеси пропорционально процентному содержанию газа и общему давлению смеси:
Для воздуха: Р атмосферное = 760 мм рт. ст.; С кислорода = 20,95%.
Оно зависит от природы газа. Всю газовую смесь атмосферного воздуха принимают за 100%, она обладает давлением 760 мм рт. ст., а часть газа (кислорода — 20,95%) принимают за х. Отсюда парциальное давление кислорода в смеси воздуха равно 159 мм рт. ст. При расчете парциального давления газов в альвеолярном воздухе необходимо учитывать, что он насыщен водяными парами, давление которых составляет 47 мм рт. ст. Следовательно, на долю газовой смеси, входящей в состав альвеолярного воздуха, приходится давление не 760 мм рт. ст., а 760 — 47 = 713 мм рт. ст. Это давление принимается за 100%. Отсюда легко вычислить, что парциальное давление кислорода, который содержится в альвеолярном воздухе в количестве 14,3%, будет равно 102 мм рт. ст.; соответственно, расчет парциального давления углекислого газа показывает, что оно равно 40 мм рт. ст.
Парциальное давление кислорода и углекислого газа в альвеолярном воздухе является той силой, с которой молекулы этих газов стремятся проникнуть через альвеолярную мембрану в кровь.
Диффузия газов через барьер подчиняется закону Фика; так как толщина мембраны и площадь диффузии одинакова, диффузия зависит от диффузионного коэффициента и градиента давления:
![]()
Q газа — объем газа, проходящего через ткань в единицу времени; S - площадь ткани; DK-диффузионный коэффициент газа; (Р 1 , — Р 2) - градиент парциального давления газа; Т — толщина барьера ткани.
Если учесть, что в альвеолярной крови, притекающей к легким, парциальное напряжение кислорода составляет 40 мм рт. ст., а углекислого газа — 46-48 мм рт. ст., то градиент давления, определяющий диффузию газов в легких, будет составлять: для кислорода 102 — 40 = 62 мм рт. ст.; для углекислого газа 40 — 46(48) = минус 6 — минус 8 мм рт. ст. Поскольку диффузный коэффициент углекислого газа в 25 раз больше, чем у кислорода, то углекислый газ более активно уходит из капилляров в альвеолы, чем кислород в обратном направлении.
В крови газы находятся в растворенном (свободном) и химически связанном состоянии. В диффузии участвуют только молекулы растворенного газа. Количество газа, растворяющегося в жидкости, зависит:
- от состава жидкости;
- объема и давления газа в жидкости;
- температуры жидкости;
- природы исследуемого газа.
Чем выше давление данного газа и температура, тем больше газа растворяется в жидкости. При давлении 760 мм рт. ст. и температуре 38 °С в 1 мл крови растворяется 2,2% кислорода и 5,1 % углекислого газа.
Растворение газа в жидкости продолжается до наступления динамического равновесия между количеством растворяющихся и выходящих в газовую среду молекул газа. Сила, с которой молекулы растворенного газа стремятся выйти в газовую среду, называется напряжением газа в жидкости. Таким образом, в состоянии равновесия напряжение газа равно парциальному давлению газа в жидкости.
Если парциальное давление газа выше его напряжения, то газ будет растворяться. Если парциальное давление газа ниже его напряжения, то газ будет из раствора выходить в газовую среду.
Парциальное давление и напряжение кислорода и углекислого газа в легких приведены в табл. 2.
Таблица 2. Парциальное давление и напряжение кислорода и углекислого газа в легких (в мм рт. ст.)
Диффузия кислорода обеспечивается разностью парциальных давлений в альвеолах и крови, которая равна 62 мм рт. ст., а для углекислого газа — это всего лишь около 6 мм рт. ст. Времени протекания крови через капилляры малого круга (в среднем 0,7 с) достаточно для практически полного выравнивания парциального давления и напряжения газов: кислород растворяется в крови, а углекислый газ переходит в альвеолярный воздух. Переход углекислого газа в альвеолярный воздух при относительно небольшой разнице давлений объясняется высокой диффузионной способностью легких для этого газа.
Парциальное давление газа в смеси газов определяется как указано выше. Парциальное давление газа, растворённого в жидкости, является парциальным давлением того газа, который образовался бы в фазе газообразования в состоянии равновесия с жидкостью при той же температуре. Парциальное давление газа измеряется как термодинамическая активность молекул газа. Газы всегда будут вытекать из области с высоким парциальным давлением в область с более низким давлением; и чем больше разница, тем быстрее будет поток. Газы растворяются, диффундируют и реагируют соответственно их парциальному давлению и не обязательно зависимы от концентрации в газовой смеси.
Законы Дальтона парциального давления
, где:= общему давлению в газовой смеси
= парциальному давлению азота (N 2)
= парциальному давлению водорода (H 2)
= парциальному давлению аммиака (NH 3)
Смеси идеальных газов
См. также
- Газ , Идеальный газ и Уравнение состояния идеального газа
Напишите отзыв о статье "Парциальное давление"
Примечания
Отрывок, характеризующий Парциальное давление
Десять человек, батальонов или дивизий, сражаясь с пятнадцатью человеками, батальонами или дивизиями, победили пятнадцать, то есть убили и забрали в плен всех без остатка и сами потеряли четыре; стало быть, уничтожились с одной стороны четыре, с другой стороны пятнадцать. Следовательно, четыре были равны пятнадцати, и, следовательно, 4а:=15у. Следовательно, ж: г/==15:4. Уравнение это не дает значения неизвестного, но оно дает отношение между двумя неизвестными. И из подведения под таковые уравнения исторических различно взятых единиц (сражений, кампаний, периодов войн) получатся ряды чисел, в которых должны существовать и могут быть открыты законы.Тактическое правило о том, что надо действовать массами при наступлении и разрозненно при отступлении, бессознательно подтверждает только ту истину, что сила войска зависит от его духа. Для того чтобы вести людей под ядра, нужно больше дисциплины, достигаемой только движением в массах, чем для того, чтобы отбиваться от нападающих. Но правило это, при котором упускается из вида дух войска, беспрестанно оказывается неверным и в особенности поразительно противоречит действительности там, где является сильный подъем или упадок духа войска, – во всех народных войнах.
Французы, отступая в 1812 м году, хотя и должны бы защищаться отдельно, по тактике, жмутся в кучу, потому что дух войска упал так, что только масса сдерживает войско вместе. Русские, напротив, по тактике должны бы были нападать массой, на деле же раздробляются, потому что дух поднят так, что отдельные лица бьют без приказания французов и не нуждаются в принуждении для того, чтобы подвергать себя трудам и опасностям.
Так называемая партизанская война началась со вступления неприятеля в Смоленск.
Прежде чем партизанская война была официально принята нашим правительством, уже тысячи людей неприятельской армии – отсталые мародеры, фуражиры – были истреблены казаками и мужиками, побивавшими этих людей так же бессознательно, как бессознательно собаки загрызают забеглую бешеную собаку. Денис Давыдов своим русским чутьем первый понял значение той страшной дубины, которая, не спрашивая правил военного искусства, уничтожала французов, и ему принадлежит слава первого шага для узаконения этого приема войны.
24 го августа был учрежден первый партизанский отряд Давыдова, и вслед за его отрядом стали учреждаться другие. Чем дальше подвигалась кампания, тем более увеличивалось число этих отрядов.
Партизаны уничтожали Великую армию по частям. Они подбирали те отпадавшие листья, которые сами собою сыпались с иссохшего дерева – французского войска, и иногда трясли это дерево. В октябре, в то время как французы бежали к Смоленску, этих партий различных величин и характеров были сотни. Были партии, перенимавшие все приемы армии, с пехотой, артиллерией, штабами, с удобствами жизни; были одни казачьи, кавалерийские; были мелкие, сборные, пешие и конные, были мужицкие и помещичьи, никому не известные. Был дьячок начальником партии, взявший в месяц несколько сот пленных. Была старостиха Василиса, побившая сотни французов.
Последние числа октября было время самого разгара партизанской войны. Тот первый период этой войны, во время которого партизаны, сами удивляясь своей дерзости, боялись всякую минуту быть пойманными и окруженными французами и, не расседлывая и почти не слезая с лошадей, прятались по лесам, ожидая всякую минуту погони, – уже прошел. Теперь уже война эта определилась, всем стало ясно, что можно было предпринять с французами и чего нельзя было предпринимать. Теперь уже только те начальники отрядов, которые с штабами, по правилам ходили вдали от французов, считали еще многое невозможным. Мелкие же партизаны, давно уже начавшие свое дело и близко высматривавшие французов, считали возможным то, о чем не смели и думать начальники больших отрядов. Казаки же и мужики, лазившие между французами, считали, что теперь уже все было возможно.
Парциальные давления дыхательных газов
Согласно закону Дальтона парциальное давление (напряжение) каждого газа в смеси (Рr) пропорционально его доле от общего объема, т.е. его фракции (Fr) . Применяя этот закон к дыхательным газам, необходимо учитывать, что атмосферный воздух, как и альвеолярная газовая смесь, содержит не только О 2 , СО 2 , N 2 и благородные газы, но и водяной пар, имеющий некое парциальное давление (Pн 2 о). Поскольку фракции газов приводятся для сухой их смеси, в уравнении для закона Дальтона из общего давления (атмосферное давление: Р атм) следует вычесть давление водяного пара. Тогда парциальное давление газа будет определяться по формуле:
Рr = Fr (Р атм - Pн 2 о)
Если подставить в уравнение парциального давления газов значения Fr для кислорода или углекислого газа в атмосферном воздухе: 21% (0,21) и 0,03% (0,0003) и давления водяного пара (47 мм рт ст), то можно вычислить, что парциальное давление указанных газов в атмосферном воздухе над уровнем моря (Р атм = 760 мм рт ст) составит, соответственно, 150 мм рт ст (20кПа) для кислорода и 0,2 мм рт ст (0,03 кПа) для углекислого газа.
Из представленной формулы следует, что снижение барометрического давления, или уменьшение удельного содержания газа (кислорода - FrО 2) во вдыхаемом воздухе будет сопровождаться падением во вдыхаемом воздухе парциального давления этого газа (кислорода - РrО 2).
Напряжение кислорода в альвеолярной газовой смеси в стандартных условиях вентиляции зависит не только от его потребления, но и от выведения углекислого газа. Соответственно, при расчете парциального давления кислорода в альвеолярной газовой смеси (Р А О 2) вносится поправка на выведение СО 2 , образующегося в процессе метаболизма. Таким образом, расчетная формула определения Р А О 2 выглядит следующим образом:
Р А О 2 = РrО 2 - ________ ,
где РаСО 2 - парциальное давление углекислого газа в артериальной крови (40 мм рт ст);
R - дыхательный коэффициент, характеризующий отношение выделенного СО 2 к поглощенному О 2 (в отсутствии стресса и при нормальном питании = 0,8).
Подставляя значения этих показателей, находим:
Р А О 2 = 150 - ________ = 100 мм рт ст (13,3 кПа)
Парциальное давление углекислого газа в альвеолярной газовой смеси составляет 40 мм рт ст (5,3 кПа). Из приведенной формулы следует, что уменьшение PrO 2 будет сопровождаться снижением Р А О 2 .
Как известно, газообмен в легких идет в направлении градиентов парциальных давлений по обе стороны альвеолярно-капиллярной мембраны (Δ). Для кислорода этот градиент соответствует разнице между Р А О 2 и напряжением кислорода в капиллярах венозной крови (40 мм рт. ст.), поступающей в легкие. Однако, за время прохождения крови через легочные капилляры (0,3 сек) это давление быстро нарастает и уже через 0,1 сек составляет ≈ 90% от величины альвеолярного давления (Г. Тевс, 2007), а в последующие 0,2 сек напряжение кислорода в капиллярах уравнивается с альвеолярным. Поэтому вводится понятие среднего градиента давления между альвеолярной газовой смесью (100 мм рт ст) и кровью легочных капилляров (90 мм рт. ст.), который составляет 10 мм рт. ст.